Modélisation du modèle vasculaire
Hind Guenou
Mon projet de recherche porte principalement sur la vascularisation des structures 3D. L’avènement de la cuture organotypique a mis en lumière les organoïdes dérivés de cellules souches ou de cellules progénitrices normales ou pathologiques. Ces entités reconstituent à une échelle beaucoup plus petite l’architecture cellulaire, spatiale et moléculaire de leurs homologues physiologiques, mimant ainsi certaines fonctionnalités de l’organe normal ou pathologique. Cependant, l’absence du microenvironnement vasculaire dans la plupart des techniques d’organoïdes limite leur utilité. En effet la vascularisation joue un rôle crucial dans le développement et la maladie. Elle constitue la niche vasculaire instructive indispensable au développement, à la fonction et à la régénération des organes (1). Elle est également nécessaire pour prévenir la nécrose. À l’heure où l’on s’oriente vers le développement d’organes bioartificiel, la capacité d’incorporer une vascularisation fonctionnelle est donc une étape essentielle dans la construction de modèles plus pertinents pour la mise en place des thérapies ciblées. Par conséquent, des stratégies de vascularisation ont été incorporées dans le but de contourner ces limites. Pour se faire, le compartiment vasculaire doit mimer la microvasculature humaine composée principalement de cellules endothéliales.
Dans ce contexte, un premier travail a été mené pour dériver des cellules endothéliales (CE) à partir d’hiPSCs (2). L’étroite relation temporelle et spatiale entre les cellules hématopoïétiques et endothéliales au cours du développement embryonnaire précoce a conduit à l’hypothèse d’un ancêtre commun (3), un précurseur hémato-endothéliale qui nous a permis de générer une population pure (> 90%) de CE au phénotype endothélial fonctionnel in vitro et in vivo dans un modèle murin d’ischémie. L’analyse des profils d’expression génique des populations dérivées des hPSCs par le système Affymetrix GeneChip, a démontré une identité moléculaire similaire à leurs homologues physiologiques respectifs isolées du foie embryonnaire humain.
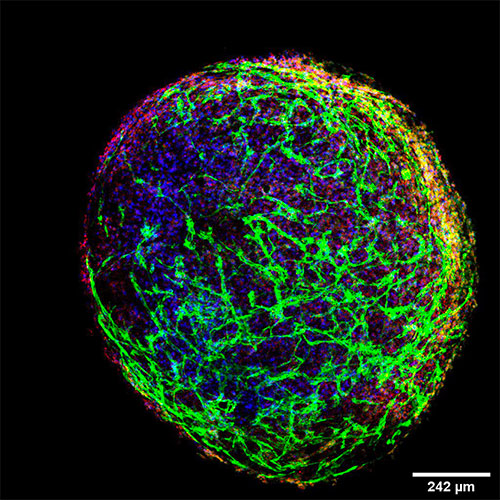
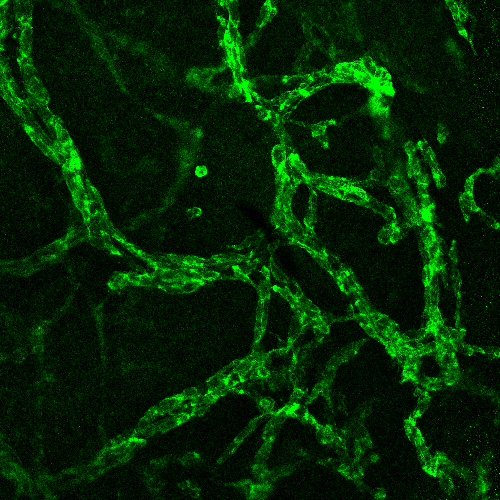
Actuellement, mon travail consiste à générer, à partir des CSPh des organoïdes de vaisseaux sanguins humains 3D, auto-organisés qui présenteraient les caractéristiques morphologiques, fonctionnelles et moléculaires des capillaires sanguins. Nous récapitulons les processus cruciaux qui régissent le développement de la vascularisation embryonnaire à savoir la vasculogénèse et l’angiogènèse.
Mon projet de recherche porte principalement sur la vascularisation des structures 3D. L’avènement de la cuture organotypique a mis en lumière les organoïdes dérivés de cellules souches ou de cellules progénitrices normales ou pathologiques. Ces entités reconstituent à une échelle beaucoup plus petite l’architecture cellulaire, spatiale et moléculaire de leurs homologues physiologiques, mimant ainsi certaines fonctionnalités de l’organe normal ou pathologique. Cependant, l’absence du microenvironnement vasculaire dans la plupart des techniques d’organoïdes limite leur utilité. En effet la vascularisation joue un rôle crucial dans le développement et la maladie. Elle constitue la niche vasculaire instructive indispensable au développement, à la fonction et à la régénération des organes (1). Elle est également nécessaire pour prévenir la nécrose. À l’heure où l’on s’oriente vers le développement d’organes bioartificiel, la capacité d’incorporer une vascularisation fonctionnelle est donc une étape essentielle dans la construction de modèles plus pertinents pour la mise en place des thérapies ciblées. Par conséquent, des stratégies de vascularisation ont été incorporées dans le but de contourner ces limites. Pour se faire, le compartiment vasculaire doit mimer la microvasculature humaine composée principalement de cellules endothéliales.
Dans ce contexte, un premier travail a été mené pour dériver des cellules endothéliales (CE) à partir d’hiPSCs (2). L’étroite relation temporelle et spatiale entre les cellules hématopoïétiques et endothéliales au cours du développement embryonnaire précoce a conduit à l’hypothèse d’un ancêtre commun (3), un précurseur hémato-endothéliale qui nous a permis de générer une population pure (> 90%) de CE au phénotype endothélial fonctionnel in vitro et in vivo dans un modèle murin d’ischémie. L’analyse des profils d’expression génique des populations dérivées des hPSCs par le système Affymetrix GeneChip, a démontré une identité moléculaire similaire à leurs homologues physiologiques respectifs isolées du foie embryonnaire humain.
Actuellement, mon travail consiste à générer, à partir des CSPh des organoïdes de vaisseaux sanguins humains 3D, auto-organisés qui présenteraient les caractéristiques morphologiques, fonctionnelles et moléculaires des capillaires sanguins. Nous récapitulons les processus cruciaux qui régissent le développement de la vascularisation embryonnaire à savoir la vasculogénèse et l’angiogènèse.
Principales publications
1. Vargas-Valderrama A, Messina A, Mitjavila-Garcia MT, Guenou H. J Biomed Sci. 2020 May 22;27(1):67. The endothelium, a key actor in organ development and hPSC-derived organoid vascularization.
2. Vargas-Valderrama A, Ponsen AC, Le Gall M, Clay D, Jacques S, Manoliu T, Rouffiac V, Ser-le-Roux K, Quivoron C, Louache F, Uzan G, Mitjavila-Garcia MT, Oberlin E, Guenou H. Endothelial and hematopoietic hPSCs differentiation via a hematoendothelial progenitor. Stem Cell Res Ther. 2022
3. Vargas-Valderrama A, Guenou H, Mitjavila Garcia MT. SL Cell Science & Report. 2019; 2(1):113. Generation of Hemangiogenic Progenitors from Human Embryonic Stem Cells
4. Guey S, Hervé D, Kossorotoff M, Ha G, Aloui C, Bergametti F, Arnould M, Guenou H, Hadjadj J, Dubois Teklali F, Riant F, Balligand JL, Uzan G, Villoutreix BO, Tournier-Lasserve E. Biallelic variants in NOS3 and GUCY1A3, the two major genes of the nitric oxide pathway, cause moyamoya cerebral angiopathy. Hum Genomics. 2023
