La thérapie cellulaire et acellulaire
du blessé de guerre
Juliette Peltzer & Marina Trouillas
Les traumatismes graves constituent un problème de santé publique majeur dans le monde. Dans le monde de la défense, les traumatismes toutes causes confondues sont la première cause de mort au combat. Les blessures balistiques ou par explosion associent des lésions diverses avec une incidence très élevée des hémorragies aigues massives et des traumatismes crâniens. La brûlure est elle aussi souvent associée aux explosions ou incendies dans des lieux confinés (véhicules, cockpit). Les conséquences physiopathologiques des traumatismes sont complexes et ne sont pas la simple somme de toutes les lésions séparées, mais plutôt un défi unique, amplifié et global pour tous les organes. Les patients souffrent souvent de pertes sanguines massives et d’attrition tissulaire entrainant coagulopathie, endothéliopathie, hyper-inflammation et déséquilibre de la réponse immunitaire, qui peuvent entraîner des défaillances multiviscérales secondaires (DMV). Ces DMV restent la principale cause de morbibité/mortalité secondaires des blessés de guerre et n’ont aucun traitement étiologique disponible. De plus, il a été observé que la formation d’ossification hétérotopique ou paraostéoarthropathie neurogènes (POAN) pouvait être une conséquence à distance d’un traumatisme, de brûlures, ainsi qu’à des lésions du système nerveux central.
La brûlure grave est une autre pathologie redoutée, notamment lors d’explosion ou incendie dans des environnements clos (navires, blindés ou aéronefs). Un élément clé de la survie est la couverture cutanée définitive. Plusieurs options chirurgicales sont envisagées, autogreffes expansées ou cultures d’épiderme autologue. Cependant, dans les brûlures très étendues, la prise de greffe reste aléatoire aboutissant souvent à une cicatrice pathologique.
Les différentes agressions subies par le blessé de guerre présentent des points communs en termes de physiopathologie et de médiateurs : troubles de l’hémostase, inflammation, signaux de souffrance cellulaire, ou dysfonctionnement de la micro ou macro-circulation. Ces grands « carrefours physiopathologiques » participent à la destruction cellulaire ou tissulaire à court terme et mènent à des anomalies de réparation. De même, les processus de réparation, même s’ils peuvent présenter des spécificités tissulaires, suivent des étapes relativement conservées : coagulation, inflammation aiguë, migration cellulaire, prolifération, différenciation, angiogenèse, synthèse et remodelage de matrice extra cellulaire.
Un outil thérapeutique permettant de moduler plusieurs des carrefours physiopathologiques conduisant aux DMV, d’améliorer la prise des greffes expansées des grands brûlés ou de prévenir la formation des POA, constituerait une stratégie innovante.
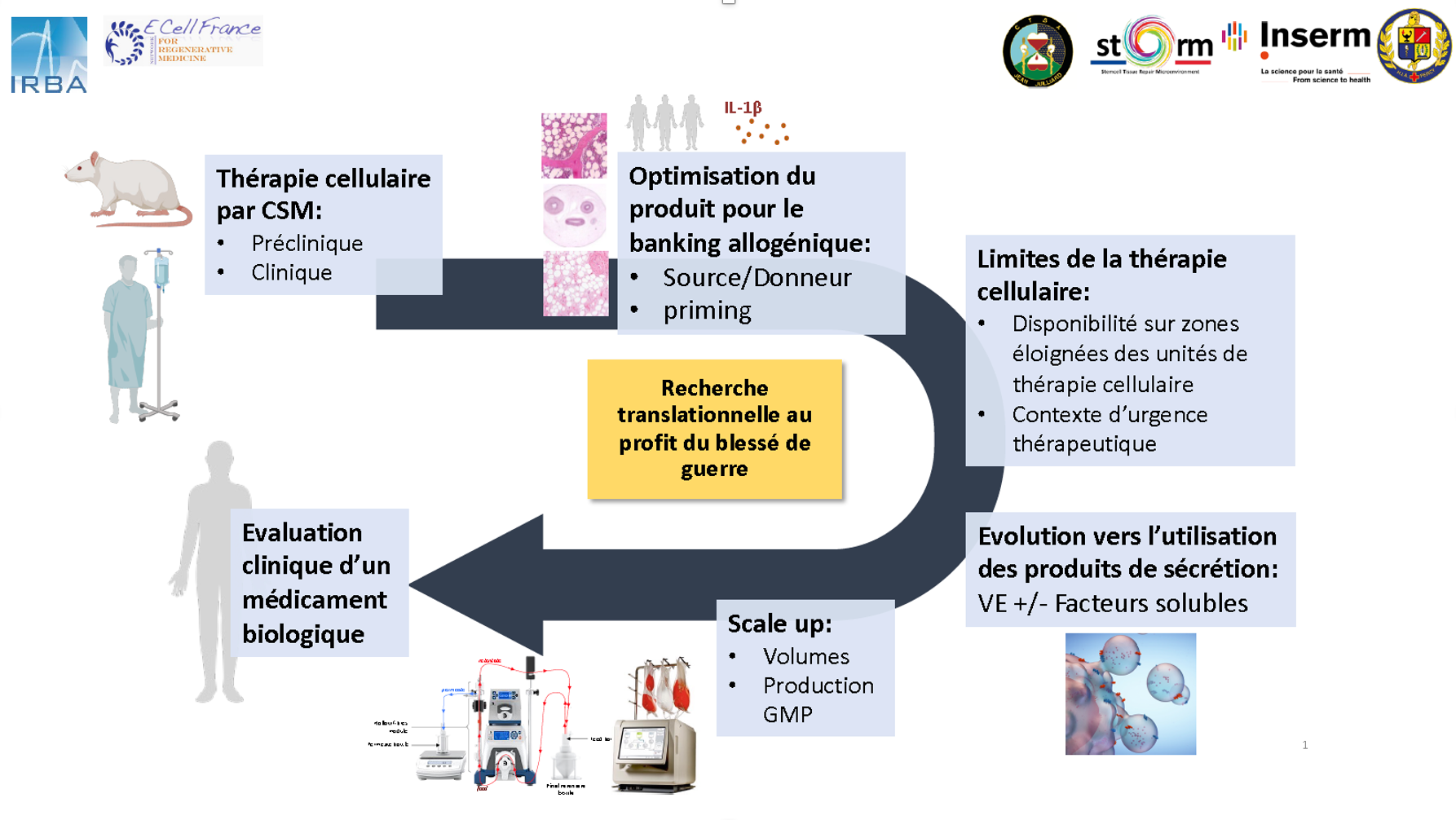
Les cellules stromales mésenchymateuses (CSM), sont utilisées en clinique comme agents thérapeutiques pour l’immunomodulation et la réparation tissulaire. Nous avons montré que l’administration systémique précoce de CSM préconditionnées à l’IL-1b limite les lésions rénales et hépatiques consécutives à un choc hémorragique sévère (Aussel et al., Stem Cell Research & Therapy, 2021). L’administration locale de CSM-IL permet aussi d’améliorer la cicatrisation cutanée via un effet anti-inflammatoire, pro-migratoire et en favorisant le remodelage matriciel (Magne et al., Journal of Investigative Dermatology, 2020).
L’efficacité des CSM est principalement attribuée à la sécrétion d’un large éventail de facteurs solubles (FS) et de des vésicules extracellulaires (VE). Au sein de l’UMR-MD-1197, nous avons adapté une méthode de Filtration à Flux Tangentiel (TFF) déjà utilisée dans l’industrie pharmaceutique, pour purifier/concentrer de grands volumes de produits de sécrétion (Lorenzini et al., Journal of Controlled Release, 2023). Ces nouveaux produits thérapeutiques acellulaires, classés comme médicaments biologiques, peuvent, contrairement aux cellules, être préparés à l’avance en grande quantité, sont faciles à conserver, à transporter et pourraient être disponibles immédiatement sur des sites éloignés des structures hospitalières. Ils représentent une formidable opportunité pour la prise en charge du blessé de guerre.
Deux grands axes en cours ont pour objectif d’évaluer et d’optimiser l’utilisation de ces produits acellulaire préparés dans des conditions compatibles avec les productions de grade clinique, pour la réparation cutanée ou la prévention des défaillances d’organes consécutives au choc hémorragique traumatique. Un dernier axe vise à comprendre la physiopathologie des POAN afin d’identifier des traitements potentiels.
Dans notre unité de recherche translationnelle nous sommes constamment confrontés aux contraintes réglementaires des productions de grade clinique, nécessitant une réflexion sur la rationalisation des sources cellulaires ainsi que leur mode préparation. Par ailleurs, la richesse des échanges avec les cliniciens nous permet de faire évoluer nos modèles fonctionnels et nos produits thérapeutiques afin qu’ils répondent au mieux et au plus vite à leurs besoins.
L’ensemble de nos projets participent à cet objectif global visant à proposer des produits acellulaires optimisés pour l’immunomodulation et la réparation tissulaire, préparés dans des conditions compatibles avec les exigences réglementaires.